FISICA
II
Serie 4
Problemas seleccionados de Calor y Primera ley de la Termodinámica
Bajar la serie en formato Word
1.-
¿Cuánto carbón se necesita para calentar el agua en un tanque de 40 galones
de 40 ° F a 180 ° F. Si el calor de combustión del carbón empleado es de
6,000 kcal/kg? (Un galón de agua pesa 8.34 lb.) Respuesta:
1.97 kg de carbón.
2.-
Si 0.04 kg de metal a 100 °C se colocan en 0.15 kg de agua a 18°
C, y la temperatura final de la mezcla es de 20 °C, ¿cuál es el
calor especifico del metal? Respuesta: 0.094
kcal/kg$°C
3.-
Si 0.08 kg de aluminio (de calor especifico 0.212) a 100 °C se colocan en 0.1
kg de agua a 15°C, ¿cuál es la temperatura final de la mezcla? Respuesta:
27.3° C
4.-
Se dan dos recipientes, uno a 80 °F y
el otro a 205 °F. ¿Cuánta agua se debe tomar de cada uno para tener 200 lb
de agua a 150 ° F? Respuesta: 88 lb de agua a 80 °F y 112 lb a 205 ° F.
5.-
¿Cuántas kilocalorías se liberan al cambiar 7.5 kg. de vapor a 100 °C a
agua a 40 ° C? Respuesta: 4,500
kcal.
6.-
Si 2 kg de metal de calor específico 0.092 a una temperatura de 190 °C se
colocan en 0.4 kg de hielo a 0 °C, ¿cuál es la temperatura final de la
mezcla? Respuesta: 5.1 ° C.
7.-
Si 0. 1 kg de vapor a 130 °C se condensa en 2.5 kg de agua a 30 °C contenida
en un calorímetro de aluminio que pesa 0.5 kg, ¿cuál es la temperatura
final de la mezcla? (Calor específico del aluminio: 0.21 cal/g$°C;
calor específico del vapor: 0.5 cal/g$°C.)
Respuesta:
51.1 °C.
8.-
¿Cuánto tiempo podrá hacerse funcionar un motor de 2,000 CV(147x104
J/s), accionando la energía liberada por 1 km3 de agua de mar
cuando la temperatura del agua desciende l °C, si todo este calor se
convirtiese en energía mecánica? ¿Por qué no se utiliza este enorme depósito
de energía? Respuesta: 28,476$105
seg = 90 años
9.-
Una casa quema 10 ton de carbón en una instalación de calefacción, siendo
las pérdidas totales de un 15 %. a) ¿Cuántas kilocalorías se utilizaron
para calentar la casa? b) En algunas localidades se calientan durante el
verano grandes depósitos de agua mediante la radiación solar, y la energía
almacenada se utiliza como calefacción durante el invierno. Calcule las
dimensiones del tanque almacén, supuesto cúbico, para almacenar una cantidad
de energía igual a la calculada en la parte a). Suponga que el agua se
calienta a 50 °C en el verano y se enfría hasta 25 °C T en el invierno. Respuesta:
a) 5,525 $
104 kcal; b) lado del tanque: l3 m.
10.-
Una muestra de 50 g de una sustancia a la temperatura de 100 °C se deja caer
dentro de un calorímetro que contiene 200 g de agua a la temperatura inicial
de 20 °C. El calorímetro es de cobre y su masa de 100 g. La temperatura
final del calorímetro es de 22 °C. Calcule el calor específico de la
muestra. Respuesta: 0.107 cal/g°$C
11.- Un vaso abierto
contiene 500 g de hielo a -20 °C. Se suministra al vaso en proporción
constante de 1,000 cal/min durante 100 min. Construya una curva tomando el
tiempo transcurrido en las abscisas y la temperatura en las ordenadas. No
tenga en cuenta la capacidad calorífica del recipiente
12.-
Un tubo une un recipiente en el que esta hirviendo agua a la presión atmosférica
con un calorímetro. La masa del calorímetro es de 150 g, su equivalente en
agua 15 g y contiene inicialmente 340 g de agua a 15°
C. El vapor se condensa en el calorímetro hasta que su temperatura
sube a 71 °C, después de lo cual la masa del calorímetro y su contenido es
de 525 g. Calcule con estos datos el calor de vaporización del agua.
Respuesta:
539 cal/g.
13.-
En un sistema doméstico de calefacción por agua caliente el agua llega a los
radiadores a la temperatura de 60 °C y sale a 38 °C. Se desea reemplaza el
sistema de calefacción por otro de vapor en el cual el vapor a la presión
atmosférica se condensa en los radiadores, saliendo de éstos a 82 °C. ¿Cuántos
kilogramos de vapor suministrarán el mismo calor que suministra 1 kg de agua
caliente en la primera instalación?
Respuesta:
0.0396 kg. de vapor.
14
.- ¿Cuántas Btu se pierden en una hora a través de una ventana de vidrio de
114 de pulg. de espesor y 24 pulg. x 48 pulg. de área, si la temperatura
exterior es de 30 °F y la interior 72 ° F? Respuesta:
9880 Btu
15.-
Un trozo de bronce de 0.01 m de espesor se expone a una temperatura de 40 °C
en un lado y de 30 °C en el otro. Si transmite 3.75 kcal en 5 min a través
de un área de 5 cm ¿cuál es la conductividad térmica del bronce? Respuesta: 0.25 kcal/m$s$°C
16
.- Una nevera eléctrica está bien aislada, excepto la puerta, que tiene 5
pulgadas de espesor, 2 pies de ancha y 4.5 pies de alta. Para conservar la
temperatura media dentro de la nevera a 38 °F cuando la temperatura del
cuarto es de 85 °F, el motor funciona durante 10 min y se detiene durante 15
min. ¿Cuántas Btu por hora remueve del interior de la nevera mientras está
funcionando el motor? El coeficiente promedio de conductividad térmica de la
puerta es 0.2 Btu$pulg/h$pie2$°F.
Respuesta: 53 Btu/h
17.-
(a) ¿Cuál es la pérdida de calor en W/m2 a través de una
ventana de vidrio de un espesor de 3.0 mm. si la temperatura del exterior es
de –5 °C y la temperatura del interior es de + 22° F.? (b) Si se instala
un cancel que tiene el mismo espesor del vidrio, pero se coloca con una
rendija de aire de 7.5 cm entre las dos ventanas, ¿cuál será la pérdida de
calor correspondiente?
18
.- Una barra de 2 m de longitud está formada por un núcleo macizo de acero
de 1 cm de diámetro, rodeado de una envoltura de cobre cuyo diámetro
exterior es de 2 cm. La superficie exterior de la barra está aislada térmicamente:
uno de sus extremos se mantiene a 100 °C y el otro a 0 °C. a) Calcule la
corriente calorífica total en la barra. b) ¿Qué fracción es transportada
por cada sustancia? Respuesta: a)
1.13 cal/seg; b) por el acero: 4 %, por el cobre: 96 %
19.-
Supóngase que la conductividad térmica del cobre es el doble de la del
aluminio y cuatro veces la del latón. Tres varillas de metal, hechas de
cobre, aluminio y latón respectivamente, tienen cada una 6.0 plg. de largo y
1.0 plg. de diámetro, Estas varillas están colocadas extremo con extremo,
estando la de aluminio entre las otras dos. Los extremos libres de las
varillas de cobre y del latón se mantienen a 100 °C y 0 °C,
respectivamente. Encontrar las temperaturas de equilibrio de la unión entre
el cobre y el aluminio y de la unión entre el aluminio y el latón.
Respuesta: Cu-Al, 86 °C; Al-latón, 57 °C.
20.-
(a) Calcular el ritmo con el que sale el calor corporal a través de la ropa
de un esquiador, a partir de los datos siguientes. La superficie de su cuerpo
es de 1.8 m2 y la ropa tiene un espesor de 1.0 cm; la temperatura
de la superficie de la piel es de 33 °C y la de la parte externa de la ropa
es de -5 °C; la conductividad térmica de la ropa es de 0.04 W/m$°K.
(b) ¿Cómo cambiaría la respuesta si, después de una caída, las ropas del
esquiador se empaparon con agua?
21.-
El calor fluye radialmente hacia afuera a través de un aislador cilíndrico
de radio exterior R2 que rodea a un tubo de vapor de radio interior
R1 donde se cumple que H=2oLk(t1-t2)/In(R2/R1).
La temperatura de la superficie interior del aislador es t, y la de la
superficie exterior es t2. ¿A qué distancia radial del centro del
tubo es la temperatura, la media aritmética de t1 y t2?
Respuesta:
(R1R2)1/2
22.-
Un chef, al despertar un día y descubrir que su estafa no funciona, decide
hervir el agua para el café de su esposa agitándola en una botella termo,
Supóngase que utiliza medio litro de agua a
28 °C, que el agua cae 1.0 pie en cada sacudida y el chef realiza 30
sacudidas cada minuto. Ignorando cualquier pérdida de calor, ¿Cuánto tiempo
debe agitar la botella para que hierva el agua?
23.-
Determinar el valor del equivalente mecánico del calor J a partir de los
siguientes datos: Se suministran 2,000 cal. a un sistema. Durante el tiempo de
suministro, el sistema efectúa un trabajo externo de 3,350 J; el aumento de
la energía interna durante el proceso es 5,030 J. Respuesta:
4.190 J/cal).
24.
(a) Calcular el posible aumento de la temperatura del agua que cae en las
cataratas del Niágara, las cuales tienen una altura de 162 pies. (b) ¿Qué
factores tenderían a impedir este posible aumento?
Respuesta:
(a) 0. 121C.
25.
En un experimento de Joule, una masa de 6.00 kg cae desde una altura de 50.0 m
y hace girar a una rueda de paletas que agita a 0.600 kg de agua. El agua está
inicialmente a 15.01 °C. ¿En cuánto aumenta su temperatura?
26.
Un atleta disipa toda la energía que le proporciona una dieta de 4,000 kcal
por día. Si tuviera que liberar dicha energía como calor a un ritmo
uniforme, ¿cómo se compararía esta producción de energía de una lámpara
de 100 W? (Nota: La caloría de nutrición es realmente una kilocaloría, tal
como la hemos definido.) Respuesta: 1.9 veces mayor.
27.
Se suministra potencia a ritmo de 0.40 hp durante 2.0 min para taladrar un
orificio en un bloque de cobre de 1.0 lb. (a) ¿Cuánto calor se genera? (b)
¿Cuál es el aumento de la temperatura del cobre si solamente el 75% de la
potencia se aprovecha para calentarlo? (c) ¿Qué sucede al 25% restante?
28.
Una bala de plomo de 2.0 g que se
mueve con una rapidez de 200 m/s , acaba incrustándose en un bloque de madera
de 2.0 kg que está suspendido como la lenteja-de un péndulo (lo que
se llama un péndulo balístico). Calcular el aumento en la temperatura de la
bala, suponiendo que toda la energía absorbida hace aumentar la temperatura
de dicha bala.
 |
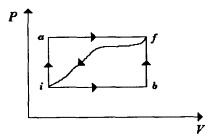
30.- Cuando un sistema
pasa del estado i al estado f a lo largo de la trayectoria iaf de la figura,
se encuentra que Q = 50 J y que W = -20 J. A lo largo de la trayectoria ibf, Q
= 36 J. a) ¿Cuál es el valor de W a lo largo de la trayectoria ibf?. b) Si W
= +13 J en la trayectoria curva
de regreso fi, ¿Cuánto vale Q en esta
trayectoria? c) Considere que Ui =10 J. Cuánto vale Uf
d) Si Ub = 22 cal, ¿Cuanto vale Q en el proceso ib?, ¿y en el
proceso bf?
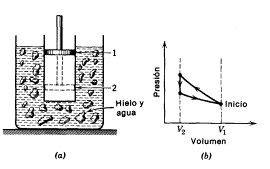
31. La figura muestra un cilindro que contiene gas y está cerrado por un émbolo móvil. El cilindro se sumerge en una mezcla de hielo y agua. Rápidamente se empuja el émbolo hacia abajo desde la posición (1) hasta la posición (2). Se mantiene el émbolo en la posición (2) hasta que el gas se encuentre de nuevo a 0"C y entonces se le levanta lentamente hasta regresar a la posición (1). La Figura es un diagrama P-V de este proceso. Si durante el ciclo se funden 100 g de hielo, ¿cuánto trabajo se ha efectuado sobre el gas? Respuesta: 8,000 cal.
32. Una bola de hierro se
deja caer sobre un piso de cemento desde una altura de 10 m. En el primer
rebote sube hasta una altura de 0.50 m. Supóngase que toda la energía mecánica
macroscópica perdida en el choque contra el suelo se queda en la bola. El
calor especifico del hierro es de 0.12 cal/g°C. Durante el choque, (a) ¿se
ha añadido calor a la bola? (b) ¿Se ha efectuado algún trabajo sobre ella?
(c) ¿Ha cambiado su energía interna? De ser así, ¿en cuánto? (d) ¿En cuánto
ha aumentado la temperatura de la bola después del primer choque? Respuesta:
(a) No. (b) Sí. (c) Sí, en + 93 J/kg. (d) 0.20 °C.
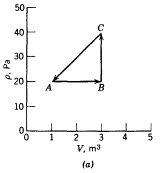
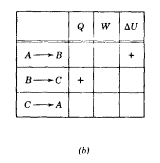
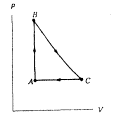
33.-
Un gas encerrado en una cámara pasa por el ciclo mostrado en la figura.
Determine el calor añadido al gas durante el proceso CA sí QAB =
20 J, QBC = 0, y WBCA= - 15 J.
34.-
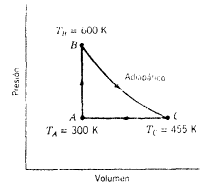
Una máquina lleva 1.00 un mol de un gas monoatomico ideal alrededor del ciclo
mostrado en la figura. El proceso AB tiene lugar a volumen constante, el
proceso BC es adiabático, y el proceso CA tiene lugar a presión constante.
(a) Calcule el calor Q, el cambio en la energía interna AU, y el trabajo W
para cada uno de los tres proceso y para el ciclo en total. (b) Sí la presión
inicial en el punto A es de 1.00 atm, halle la presión y el volumen en los
puntos B y C. Use 1 atm = 1.0 13 $
105 Pa y R = 8.314 J/mol$
°K.
FISICA II
Profesor: M.C. Luis Alfonso Domínguez Carballo
INVESTIGACION
DOCUMENTAL
TEMAS:
1. Teoría cinética
de los gases ideales
1.1
Descripciones macroscópicas y microscópicas de un gas ideal
1.1.1.
Ley de Boyle
1.1.2.
Ley Marriote
1.1.3. Ley Gay Lussac
1.1.4.
Ecuación de estado del Gas ideal
1.2
Calor especifico de un gas ideal a volumen constante y a presión
constante
1.2 Interpretación cinética de la temperatura
2.
La Segunda ley de la Termodinámica
2.1.- Procesos reversibles e irreversibles.
2.2.- Segunda ley de la termodinámica.
2.3.- Ciclo de Carnot.
2.4.- Máquinas térmicas (Ciclo Rankine, Otto y
Diesel).
2.5.- La Segunda ley de la termodinámica y la Entropía.
2.6.- La Entropía y desorden.
BIBLIOGRAFÍA
-
Resnick, R. y Hallyday, D., FÍSICA Parte 1, CECSA, 1997.
-
Serway, R. A., FÍSICA Tomo I, McGraw-Hill, 1993.
-
Sears, F. W., Zemansky, M. W. y Young, H. D., FÍSICA UNIVERSITARIA, Addison-Wesley Iberoamericana, S.A., 1988.
-
Kikoin, A. K. y Kikoin, I. K., FÍSICA MOLECULAR, ed. MIR, Moscú.
-
Tipler P. A., FÍSICA Tomo I, Reverté, 1993.
-
Los demás ( libros, enciclopedias, Internet, etc...)